Xinhua News Agency, Tianjin (Reporter Zhang Jianxin, Li Yating) Il team di Liu Shulin, ricercatore presso la Scuola di Chimica dell'Università di Nankai in Cina, ha recentemente sviluppato con successo un nuovo percorso del virus anti-influenzale ad ampio spettro. Questa strategia interrompe radicalmente il vantaggio evolutivo del virus degradando in modo sincrono più componenti chiave al centro della replicazione virale, ponendo solide basi per lo sviluppo della prossima generazione di farmaci anti-influenzali potenti, durevoli e ad ampio spettro. Risultati di ricerca rilevanti sono stati recentemente pubblicati sulla rivista accademica internazionale "Journal of the American Chemical Society".
Secondo il gruppo di ricerca, i virus dell'influenza A possono facilmente eludere le risposte immunitarie dell'ospite e i farmaci esistenti a causa del loro elevato tasso di mutazione. Gli attuali farmaci antivirali utilizzati clinicamente possono solitamente colpire solo un singolo bersaglio del virus, il che rende facile per il virus sviluppare resistenza ai farmaci attraverso la mutazione, con conseguente effetto del farmaco notevolmente ridotto e efficacia limitata ad ampio spettro. Sono urgentemente necessarie nuove strategie terapeutiche in tutto il mondo.
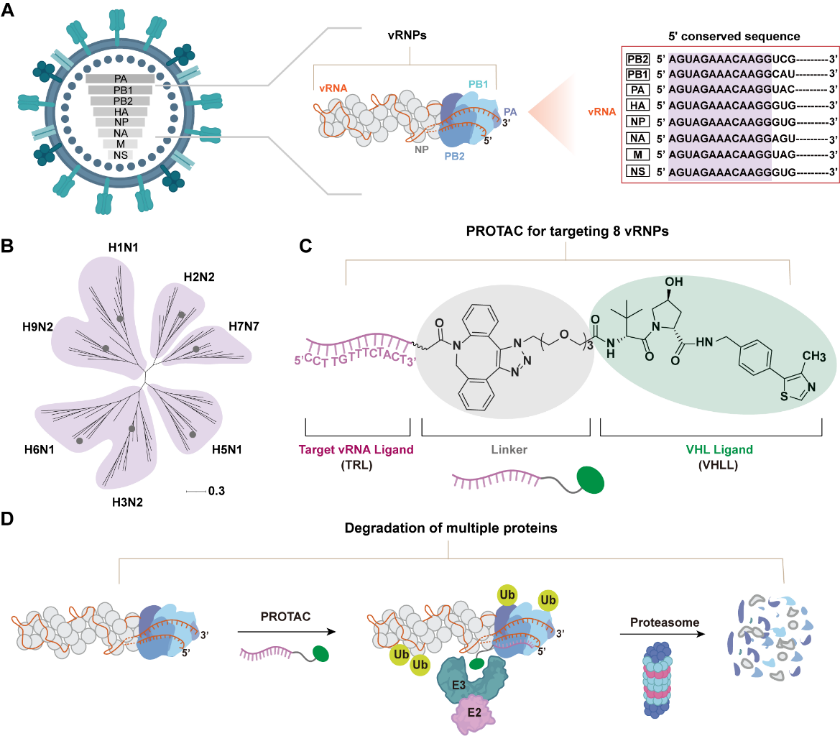
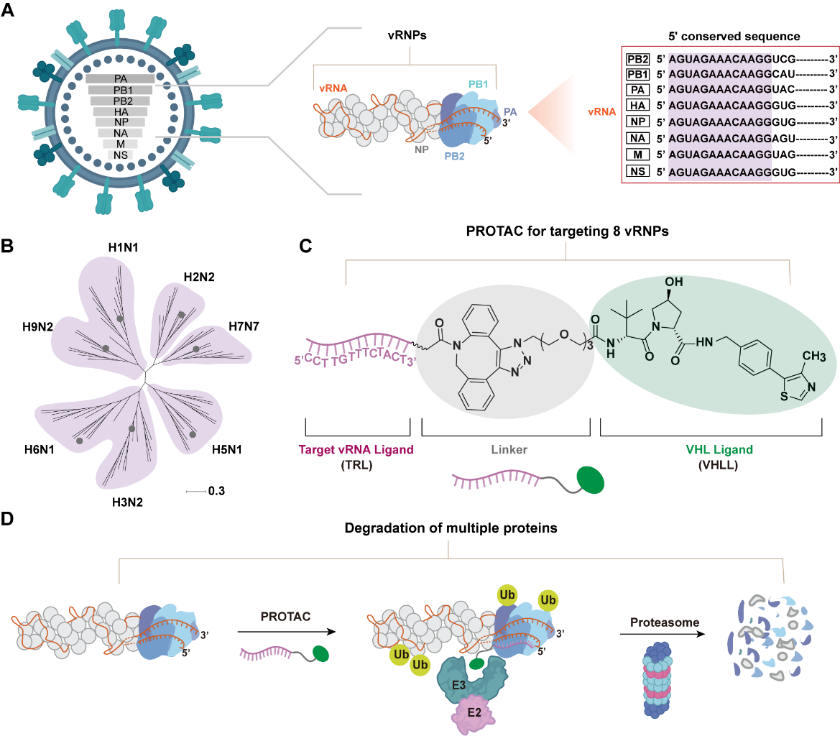
Diagramma schematico della degradazione mediata da PROTAC delle proteine multivirali. L'agenzia di stampa Xinhua ha riferito che Liu Shulin ha riferito che il team ha sviluppato una strategia anti-virus chiamata "Multiplex PROTAC". Il suo meccanismo principale risiede nell'uso intelligente di una regione 5' non tradotta altamente conservata nel targeting dell'RNA virale, che è considerato il "codice universale". Sulla base di ciò, i ricercatori del loro team hanno progettato una molecola PROTAC multifunzionale. Un'estremità della molecola può riconoscere e legare con precisione il "codice universale" del virus, mentre l'altra estremità è responsabile del reclutamento del proteasoma, il sistema di degradazione delle proteine intrinseco nelle cellule umane. Questo design fa sì che la molecola si comporti come un "cavallo di Troia". Dopo essere entrato in una cellula infetta, può agganciarsi al complesso ribonucleoproteico virale, il nucleo della replicazione virale e allo stesso tempo il "frantumatore" della cellula, contrassegnando così la proteina centrale del virus come un segno di "distruzione" e quindi guidando il macchinario cellulare a degradare completamente queste parti chiave per la replicazione virale, distruggendo la capacità di replicazione del virus fin dall'origine.
I risultati sperimentali del team mostrano che la strategia multipla PROTAC mostra eccellenti prestazioni antivirali. Non solo può inibire efficacemente la replicazione virale in modo concentrazione-dipendente, ma il suo effetto inibitorio può durare più di 48 ore. La sua persistenza ed efficacia sono significativamente migliori rispetto ai farmaci di controllo a bersaglio singolo. Ciò che è particolarmente critico è che questa strategia costruisce con successo un’elevata barriera di resistenza genetica degradando in modo sincrono più proteine virali. Ciò significa che se il virus vuole fuggire, deve avere mutazioni di fuga efficaci su più bersagli chiave contemporaneamente. Ciò costituisce un ostacolo insormontabile per il virus nell’evoluzione naturale e riduce il rischio di resistenza ai farmaci. Inoltre, questa strategia ha mostrato un’attività ad ampio spettro contro più ceppi influenzali, evidenziandone il potenziale come farmaco anti-influenzale ad ampio spettro.
I revisori hanno commentato che la versatilità di questa strategia fornisce anche un nuovo percorso tecnico e spazio di immaginazione per affrontare in futuro altri virus in rapida mutazione.